Un trastorno que puede ser un importante desafío clínico. En general, el pronóstico de la PMR es bueno y la enfermedad se cura en algunos años, durante los cuales se debe indicar glucocorticoides para controlar la enfermedad y sus síntomas.
por I. Lundberg, A. Sharma, C. Turesson y A. Mohammad Journal of Internal Medicine, 2022, 00; 116
- Resumen
- Epidemiología
- Patogénesis y fisiopatología
- Presentación clínica y curso de la enfermedad
- Asociación con arteritis temporal
- Criterios de diagnóstico y clasificación
- Diagnóstico
- Estudios de imagen
- Hallazgos de laboratorio
- Diagnóstico diferencial
- PMR como un evento relacionado con el uso de inhibidores de puntos de control inmunitario en el tratamiento del cáncer
- Tratamiento
- Comorbilidades
- Mortalidad
- Conclusión
- Referencia bibliográfica

Resumen, traducción y comentario objetivo: Dr. Cristian Pisa
Resumen
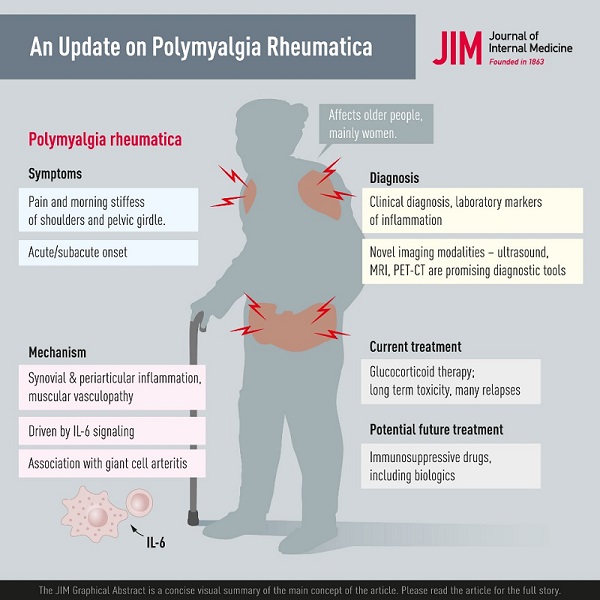
La polimialgia reumática (PMR) es la enfermedad reumática inflamatoria más común que afecta a personas mayores de 50 años y es 2 a 3 veces más común en mujeres. Los síntomas más comunes son dolor y rigidez matinal en la cintura escapular y pélvica y el inicio puede ser agudo o desarrollarse en unos pocos días o semanas. Pueden presentarse síntomas generales como fatiga, fiebre y pérdida de peso, probablemente provocados por la señalización sistémica de IL-6.
La patología incluye inflamación sinovial y periarticular y vasculopatía muscular. Una nueva observación es que la PMR puede aparecer como un efecto secundario del tratamiento del cáncer con inhibidores de puntos de control. El diagnóstico de PMR se basa principalmente en síntomas y signos combinados con marcadores de laboratorio de inflamación.
Las modalidades de imagen, incluyendo ultrasonido, resonancia magnética y tomografía por emisión de positrones son prometedoras en la investigación de la sospecha de PMR. Sin embargo, todavía están limitadas por la disponibilidad, el alto costo y el rendimiento poco claro en el trabajo de diagnóstico.
La terapia con glucocorticoides (GC) es eficaz en la PMR y la mayoría de los pacientes responde rápidamente a 15 a 25 mg de prednisolona por día. Existen desafíos en el manejo de pacientes con PMR, ya que hay recaídas y es posible que los pacientes con PMR deban permanecer con GC durante períodos prolongados. Esto se asocia con altas tasas de comorbilidades relacionadas con GC, como diabetes y osteoporosis, y hay datos limitados sobre el uso de fármacos antirreumáticos modificadores de la enfermedad y productos biológicos como agentes ahorradores de GC.
Finalmente, la PMR se asocia con arteritis de células gigantes, que puede complicar el curso de la enfermedad y requerir un tratamiento más intenso y prolongado.
Epidemiología
La polimialgia reumática (PMR) es un trastorno reumático asociado con dolor musculoesquelético y rigidez en el área del cuello, los hombros y la cadera. La etiología no se comprende del todo, pero existen factores ambientales y genéticos asociados.
La incidencia de PMR aumenta con la edad y rara vez se observa en personas menores de 50 años. Las mujeres tienen aproximadamente 2 a 3 veces más probabilidades de verse afectadas.
La PMR es de 2 a 3 veces más común que la arteritis de células gigantes (ACG) y ocurre en aproximadamente el 50 % de los pacientes con ACG. La PMR puede preceder, acompañar o seguir a la ACG.
La incidencia es más alta en los países escandinavos y las personas de ascendencia del norte de Europa. La incidencia estimada y la prevalencia de PMR son considerablemente más bajas en otras partes del mundo, aunque todos los grupos raciales y étnicos pueden verse afectados.
Se están investigando varias causas potenciales de PMR. Algunas de las teorías involucran la variante genética HLA-DR4. Los subtipos de HLA-DR4 se han asociado con la artritis reumatoidea (AR), y dichos alelos también están presentes en muchos casos en los que la PMR y la ACG ocurren juntas. Se sospecha que el inicio repentino de la PMR y la naturaleza de los síntomas como dolor en las articulaciones, fiebre y malestar general son el resultado de infecciones causadas por virus.
El daño a las arterias superficiales por la alta exposición a la radiación ultravioleta del sol es otra causa propuesta para el desarrollo de PMR. Algunos estudios sugieren que las fibras elásticas presentes en las arterias y las membranas sinoviales son dañadas por los rayos ultravioleta. Estos tejidos dañados pueden infectarse con virus que permanecen inactivos durante mucho tiempo y pueden reactivarse más tarde, causando PMR. Su inicio repentino y la amplia variación en la incidencia reportada en varias partes del mundo sugieren la contribución de uno o más agentes ambientales, factores genéticos, o ambos,
También se ha sugerido que la PMR y la ACG pueden ser desencadenadas por la vacunación contra la influenza estacional. Otro estudio informó el primer caso de un síndrome similar a PMR 7 días después de la vacunación. No obstante, varios estudios han informado que los síntomas generalmente se resuelven rápidamente en tales casos.
Patogénesis y fisiopatología
Los síntomas típicos de dolor muscular proximal y rigidez en la PMR pueden explicarse por inflamación sinovial y periarticular en las articulaciones centrales. Las biopsias de pacientes con PMR no tratados han demostrado sinovitis con infiltración de leucocitos (macrófagos y células T de memoria, y algunas células B) y proliferación vascular.
Además, la activación del endotelio vascular puede ser importante para la patogenia, ya que se ha observado un aumento de la expresión del factor de crecimiento endotelial vascular (VEGF) en las biopsias sinoviales. Esto puede contribuir al reclutamiento de células inflamatorias en estas lesiones. Se ha demostrado que el péptido intestinal vasoactivo (VIP) se expresa en mayor medida en la membrana sinovial de pacientes con PMR en comparación con aquellos con AR u osteoartritis. Se ha sugerido que la nocicepción relacionada con la producción local de VIP puede contribuir a las molestias típicas en el hombro de la PMR.
Además, las investigaciones ecográficas han revelado bursitis subacromial-subdeltoidea y tendinitis de la porción larga del bíceps braquial en la mayoría de los pacientes con PMR. La microscopía por inmunofluorescencia de biopsias de dicho músculo ha demostrado depósitos de fibrinógeno e IgA en el área perifascicular del perimisio. Se ha observado un aumento de la microvascularización muscular en la PMR temprana no tratada.
Se ha demostrado que los niveles plasmáticos de IL-6, pero no de TNF-α, están elevados tanto en la ACG como en la PMR. La fuente principal de esta liberación de IL-6 son las células T CD4+. Además, se ha demostrado que los niveles circulantes del receptor soluble de IL-6 predicen futuras recaídas en pacientes con PMR, lo que subraya aún más la importancia de la señalización de IL-6 en este contexto.
Las perturbaciones de los subconjuntos de células T y células B circulantes se han descrito en la PMR, pero con resultados inconsistentes. Dado que la PMR es una enfermedad de las personas mayores, estos patrones pueden reflejar el envejecimiento del sistema inmunitario. Se han observado recuentos elevados de monocitos en sangre periférica tanto en PMR como en ACG, con una disminución significativa después del tratamiento en PMR, pero no en ACG. En contraste con muchos otros trastornos reumáticos, ningún autoanticuerpo se ha asociado consistentemente con PMR o ACG. La evidencia combinada apoya una interacción entre el sistema inmunitario celular innato y adaptativo.
Mientras que se ha demostrado que las características metabólicas (IMC más bajo, niveles más bajos de glucosa en ayunas) que pueden contribuir a la regulación inmunitaria están asociadas con el desarrollo posterior de ACG, la relación entre dichos factores y el riesgo de PMR ha aún no ha sido investigado.
Presentación clínica y curso de la enfermedad
Un rasgo característico de la PMR es una aparición nueva y relativamente aguda de dolor muscular proximal y rigidez en el cuello, los hombros, la parte superior de los brazos, las caderas y los muslos. Los pacientes a menudo sufren de una rigidez matutina pronunciada con dificultad para acostarse o levantarse de la cama por la mañana con algún alivio espontáneo de los síntomas más tarde en el día. La rigidez afecta incluso a otras actividades físicas por la mañana, como vestirse o realizar otras actividades diarias.
Los síntomas generalmente se desarrollan por completo en unos pocos días a un par de semanas. En ocasiones, el inicio es más insidioso y puede dar lugar a síntomas inespecíficos como fatiga, artralgias, pérdida de apetito, pérdida de peso o fiebre. No es inusual que algunos pacientes se sometan a investigaciones por sospecha de enfermedad maligna antes de que se pueda realizar el diagnóstico con PMR.
La presentación clínica inespecífica y la ausencia de hallazgos de laboratorio o características serológicas específicas a menudo conducen a algún retraso en el diagnóstico.
La PMR impone una carga importante en la vida diaria de las personas mayores. El impacto psicológico es significativo, incluida la ansiedad relacionada con la enfermedad activa y los efectos secundarios del tratamiento con glucocorticoides (GC).
Asociación con arteritis temporal
La PMR y la arteritis temporal (AT) a menudo coexisten, lo que sugiere factores predisponentes compartidos y mecanismos de enfermedad compartidos. Dado que la histopatología típica de la AT en biopsias de dicha arteria incluye la presencia de células gigantes, la enfermedad a menudo se denomina ACG.
La arteritis de células gigantes (ACG) es una vasculitis sistémica que puede afectar a varios vasos grandes, incluyendo a menudo, aunque no siempre, la arteria temporal.
Debe sospecharse un diagnóstico concomitante de ACG en un paciente con PMR que además padezca cefalea de nueva aparición, claudicación mandibular, síntomas visuales nuevos e inexplicables o síntomas constitucionales graves (fiebre de origen desconocido, pérdida de peso, fatiga, etc.). Dichos síntomas pueden ocurrir en la primera presentación con PMR o más tarde durante el curso de la enfermedad.
La arteritis subclínica también puede ocurrir en pacientes con PMR. En estudios sistemáticos de pacientes con un fenotipo clínico típico de PMR, pero sin signos o síntomas compatibles con la ACG, se encontraron hallazgos histopatológicos de vasculitis en biopsias de la arteria temporal hasta en un 21 %, y características ecográficas de AT en hasta un 32 %. La recurrencia de los síntomas de la PMR es una característica común de la recaída de la ACG.
Criterios de diagnóstico y clasificación
Muchos criterios diagnósticos diferentes han sido propuestos. El propósito de estos criterios es ayudar a los médicos a realizar el diagnóstico de PMR en pacientes individuales. La mayoría de estos criterios se basan en las características demográficas, clínicas y de laboratorio de la PMR. Los criterios EULAR/ACR se resumen en la Tabla 1. Los criterios de clasificación están destinados a ser utilizados en estudios epidemiológicos y no para hacer un diagnóstico en pacientes individuales.
Tabla 1. Criterios de clasificación provisional EULAR/ACR para la polimialgia reumática (Modificado de Dasgupta et al.)

Criterios requeridos: edad ≥50 años, dolor de hombro bilateral y proteína C reactiva anormal y/o velocidad de sedimentación globular.
* Sin/con ultrasonido.
Abreviaturas: Anti-CCP, anticuerpo antipéptido cíclico citrulinado; ACR, Colegio Americano de Reumatología; EULAR, Alianza Europea de Asociaciones de Reumatología; FR, factor reumatoide.
La sensibilidad y especificidad de los criterios varían dependiendo de si el PMR discrimina todas las condiciones, incluida la RA o las condiciones que afectan a los hombros. La sensibilidad y la especificidad también varían según se utilice o no la ecografía. Una puntuación ≥4 tuvo una sensibilidad del 68 % y una especificidad del 78 %. Al discriminar las condiciones del hombro en PMR, la especificidad aumentó al 88 %, mientras que fue solo del 65 % para discriminar la AR de la PMR. Mediante ecografía, una puntuación ≥5 tenía una sensibilidad del 66 % y una especificidad del 81 %.
Diagnóstico
No existe un estándar de oro para diagnosticar la PMR y, a diferencia de muchos otros síndromes reumáticos, no hay manifestaciones clínicas específicas, serología u otros hallazgos de laboratorio. Como resultado, el diagnóstico puede ser un desafío.
| Diagnóstico En la práctica diaria, el diagnóstico de PMR se basa principalmente en la siguiente combinación: síntomas de nueva aparición de rigidez matinal y dolor en la cintura escapular y pélvica en una persona de 50 años o más, evidencia de inflamación sistémica con un aumento de la velocidad de sedimentación globular (VSG) y/o PCR, ninguna otra enfermedad que explique mejor la presentación clínica y finalmente respuesta abrupta a los GC. En algunos criterios diagnósticos, existen otros requisitos específicos, como una duración de los síntomas de 2 semanas o pruebas negativas para factores reumatoides o anticuerpos antinucleares. |
El diagnóstico de PMR debe considerarse clínicamente.
El caso típico es el de una anciana con dolor y rigidez bilateral en el hombro a primera hora de la mañana. Síntomas similares a menudo ocurren en la cintura pélvica. Por lo general, los síntomas se alivian durante el día. Las manifestaciones sistémicas como fiebre, fatiga, pérdida de apetito y pérdida de peso pueden ocurrir en aproximadamente un tercio de los pacientes.
Otros parámetros inflamatorios pueden estar elevados como glóbulos blancos o recuento de plaquetas y, a veces, las enzimas hepáticas o la fosfatasa alcalina pueden estar elevadas como un signo de inflamación sistémica. En el examen clínico, a menudo se observa sensibilidad a la palpación profunda de los músculos alrededor de los hombros y los muslos. Además, suele haber movilidad restringida en los hombros, sin atrofia o debilidad muscular. Pueden verse signos ocasionales de sinovitis en los hombros, las articulaciones de las muñecas y las rodillas. Finalmente, en la PMR, la mayoría de los pacientes responderán rápida y dramáticamente a los GC y, según algunos criterios, esta respuesta es necesaria para el diagnóstico.
Estudios de imagen
Debido a los síntomas inespecíficos o los hallazgos de laboratorio de la PMR, existe una necesidad insatisfecha de otras modalidades para confirmar el diagnóstico. Se han utilizado varias modalidades de imagen en la PMR, incluida la radiología convencional, la gammagrafía, la tomografía computarizada (TC), la resonancia magnética nuclear (RMN), la ecografía y la tomografía por emisión de positrones con TC (PET CT).
El objetivo de los estudios de imagen en la PMR no es solo confirmar el diagnóstico, sino también descartar diagnósticos diferenciales o comorbilidades y, en algunos casos, la coexistencia con vasculitis de grandes vasos.
La ecografía es útil en la PMR debido a la naturaleza de la afectación de los tejidos blandos extraarticulares. Los hallazgos más comunes son inflamación y derrame de la bursa subacromial-subdeltoidea, tenosinovitis del bíceps, inflamación de la articulación glenohumeral y sinovitis y trocanteritis de cadera. La ecografía también es útil para descartar otros diagnósticos diferenciales y para detectar vasculitis de grandes vasos y arteritis craneal cuando se sospecha que coexisten con la PMR.
También se ha utilizado la RMN, aunque su uso todavía está limitado la investigación. Los hallazgos incluyen un patrón característico de inflamación simétrica en el trocánter mayor, el acetábulo y la tuberosidad isquiática, informado en el 64 % de los pacientes con PMR en un estudio. En otro estudio, todos los pacientes con PMR de inicio reciente tenían al menos un sitio de inflamación miofascial. Las ventajas de la resonancia magnética sobre la ecografía incluyen que la resonancia magnética es más específica con menos variación entre observadores en la evaluación de la vasculitis. Las desventajas incluyen la disponibilidad y el costo.
La PET CT se ha utilizado en oncología y en la investigación de enfermedades inflamatorias. En pacientes con sospecha de PMR, no se recomienda el uso de PET CT como examen de rutina debido a limitaciones como el costo y la disponibilidad. Además de su papel en la visualización de la inflamación en los tejidos articulares y extraarticulares, la PET CT es extremadamente útil para confirmar la sospecha de vasculitis de grandes vasos y la diferenciación entre la PMR y otras afecciones, como tumores malignos u otras enfermedades reumáticas. Se justifica su uso en pacientes que no respondieron al tratamiento inicial con GC. La falta de respuesta podría explicarse por vasculitis de grandes vasos coexistente, otras enfermedades reumáticas subyacentes o malignidad.
> Otros estudios de imagen
La radiografía convencional se ha utilizado anteriormente en este contexto, especialmente en pacientes con sospecha de PMR y enfermedad articular periférica. La artritis en la PMR no suele ser erosiva, lo que la distingue de la artritis destructiva típica de la AR u otras enfermedades artríticas como la condrocalcinosis. La gammagrafía no se usa actualmente.
Hallazgos de laboratorio
No existen hallazgos serológicos u otros hallazgos de laboratorio específicos que puedan confirmar el diagnóstico de PMR con absoluta certeza.
El hallazgo más frecuente e importante es la elevación de parámetros inflamatorios como la VSG o la PCR. Sin embargo, una VSG normal no excluye el diagnóstico de PMR. Otros hallazgos incluyen anemia normocítica normocrómica, trombocitosis y leucocitosis.
Diagnóstico diferencial
Las condiciones que afectan a personas en el grupo de edad de 50 años o más y que se asocian con dolor de hombro bilateral deben incluirse en los diagnósticos diferenciales de la PMR. El diagnóstico diferencial debe incluir tanto enfermedades reumáticas como no reumáticas.
> Artritis reumatoidea
Entre las condiciones reumáticas más importantes en el diagnóstico diferencial de la PMR se encuentra la AR seronegativa. Esto es especialmente cierto al inicio de la enfermedad de la AR, que podría tener una fase prodrómica de artritis bilateral de la articulación del hombro. Además, tanto la AR como la PMR pueden presentarse con artritis en las articulaciones de la muñeca, y si los pacientes tienen un resultado negativo para el factor reumatoide y/o el péptido anticíclico citrulinado (anti-CCP), la diferenciación entre estas dos condiciones puede no ser fácil.
Sin embargo, la presencia de artritis simétrica de pequeñas articulaciones debería favorecer el diagnóstico de AR. Tanto la AR como la PMR se pueden tratar con éxito con prednisolona, lo que limita la utilidad de este medicamento en la diferenciación. Las manifestaciones extraarticulares típicas (p. ej., nódulos reumatoides, vasculitis cutánea, serositis, etc.) y FR/anti-CCP positivos favorecen el diagnóstico de AR más que de PMR.
> Miositis
La polimiositis (PM) es otra enfermedad que puede ser mal diagnosticada como PMR y viceversa. Ambas condiciones afectan los grupos musculares proximales en las extremidades superiores e inferiores. Sin embargo, la presencia de debilidad muscular en lugar de rigidez y dolor es una característica diferencial importante de la PM. Además, la PM generalmente se asocia con niveles séricos elevados de enzimas musculares, lo que no es una característica de la PMR. Otras características que favorecen la posibilidad de PM es la presencia de autoanticuerpos específicos de miositis y manifestaciones extramusculares. La dificultad para tragar favorecerá el diagnóstico de PM. La debilidad muscular pura no es típica de la PMR.
> Síndromes de dolor
La diferenciación entre PMR y síndromes de dolor como la fibromialgia debería ser más fácil en comparación con otros diagnósticos diferenciales. La fibromialgia generalmente tiene su inicio en grupos de edad más jóvenes. Además, no hay elevación de los parámetros de laboratorio que indiquen una condición inflamatoria. Es importante diferenciar entre estas dos condiciones para evitar el uso innecesario de GC en pacientes con fibromialgia y síndromes de dolor.
> Malignidad
Un diagnóstico diferencial importante en la PMR son las enfermedades malignas.
Las manifestaciones de PMR podrían representar un síntoma paraneoplásico. Los pacientes con PMR que no responden a una dosis diaria de prednisolona de 15 a 25 mg o que tienen una recurrencia rápida de los síntomas directamente después de la reducción gradual de los GC deben alertar al médico tratante sobre la posibilidad de una enfermedad maligna subyacente.
La sinovitis simétrica seronegativa remitente con edema con fóvea es un síndrome clínico caracterizado por la aparición de artritis simétrica de articulaciones pequeñas con edema de las manos y los pies, típicamente en hombres de edad avanzada con factor reumatoide negativo. Esta condición generalmente responde bien a un curso corto de GC orales y debe ser uno de los diagnósticos diferenciales importantes para la PMR. Se puede observar un fenotipo similar en los síndromes paraneoplásicos.
> Otros
Las enfermedades degenerativas no inflamatorias, como la espondilosis cervical y la osteoartritis de la articulación de la cadera, pueden simular la presentación de la PMR con síntomas como dolor y rigidez matutina. La confirmación radiológica de osteoartrosis (OA) o espondilosis junto con la ausencia de parámetros inflamatorios activos favorecerá el diagnóstico de espondilosis y OA en lugar de PMR. El hipotiroidismo es una enfermedad común en mujeres con dolor difuso, fatiga y un síndrome similar a la fibromialgia.
PMR como un evento relacionado con el uso de inhibidores de puntos de control inmunitario en el tratamiento del cáncer
Los inhibidores de puntos de control inmunitario (ICI) se utilizan cada vez más en la terapia contra el cáncer para potenciar la respuesta inmunitaria antitumoral. El tratamiento con anticuerpos monoclonales que bloquean la proteína CTLA-4, el receptor (PD-1) o su ligando PD-L1, se ha asociado con la aparición de una serie de enfermedades autoinmunes. La PMR es uno de los trastornos reumáticos que se ha informado como un evento relacionado en este contexto.
Además, existen varios informes sobre casos con ‘enfermedad similar a la PMR’, con algunas características atípicas, después del tratamiento con ICI. La caracterización cuidadosa de tales casos podría guiarnos en la comprensión del papel del sistema inmunitario adaptativo en la fisiopatología de la PMR.
Tratamiento
> GC orales
La piedra angular en el tratamiento de la PMR son los GC orales. Todos los síntomas de PMR generalmente responden rápidamente a los GC. La dosis inicial diaria recomendada de prednisolona en PMR es de 12,5 a 25 mg según la recomendación ACR/EULAR más reciente. Una dosis inicial de 20 mg es superior a 10 mg pero a costa de más eventos adversos. La elección dentro del intervalo de 12,5 a 25 mg debe considerar la actividad inflamatoria, el riesgo de recaída y el riesgo de toxicidad por GC debido a comorbilidades como diabetes o enfermedad cardiovascular.
La dosis de prednisolona debe reducirse gradualmente en alrededor de 2,5 mg por mes hasta 10 mg por día, después de lo cual continúa la disminución más lenta. Una mala respuesta al tratamiento debe llevar a reconsiderar posibles diagnósticos diferenciales. El tratamiento con GC debe ir acompañado de medidas de apoyo para minimizar la toxicidad a largo plazo, como la osteoporosis.
En general, el pronóstico de la PMR es bueno y, por lo general, la enfermedad se cura en un par de años, durante los cuales se debe tomar GC para controlar la enfermedad y sus síntomas. Algunos pacientes tienen una evolución más complicada con inflamación residual durante el tratamiento y recurrencia de los síntomas al intentar reducir la dosis de GC. En un estudio realizado por Healey, solo el 30 % de los pacientes pudieron suspender el tratamiento con GC y permanecer asintomáticos dentro de los 2 años posteriores al seguimiento, mientras que solo el 2 % pudo detener el GC por completo dentro de los 6 meses.
> GC inyectable
La metilprednisolona intramuscular (MPim) se ha comparado con los GC orales en el tratamiento de la PMR en cuanto a eficacia y seguridad. En un estudio realizado por Dasgupta et al., la tasa de remisión después de una fase doble ciego de 12 semanas fue similar, pero la dosis media acumulada de GC en el grupo de metilprednisolona intramuscular después de 96 semanas fue el 56 % de la del grupo GC orales. El grupo que utilizó la vía IM tuvo menos eventos no deseados a largo plazo. La MPim es probablemente una alternativa adecuada a los GC orales en pacientes de edad avanzada con múltiples medicamentos, así como en pacientes que experimentan un problema siguiendo el programa de reducción gradual de los GC orales y en pacientes con problemas de adherencia.
> Fármacos y productos biológicos antirreumáticos modificadores de la enfermedad
Debido a la toxicidad de la terapia con GC a largo plazo, existe una clara necesidad de estrategias alternativas en pacientes con PMR. Sin embargo, los fármacos antirreumáticos que han tenido un gran éxito en el tratamiento de la AR y varios otros trastornos reumáticos, no se han estudiado ampliamente en la PMR.
Existe cierta evidencia de beneficio del metotrexato (MTX) en pacientes con PMR. En un ensayo controlado aleatorizado (ECA) doble ciego, se demostró un menor riesgo de recaída y una mayor probabilidad de interrupción de GC en pacientes con PMR de nueva aparición que tomaban MTX además de un régimen regular de GC en comparación con el grupo de comparación que tomaba GC + placebo. No se ha evaluado sistemáticamente la eficacia del MTX en la PMR recurrente y de larga evolución.
Con base en este tipo de evidencia, el panel ACR/EULAR recomendó condicionalmente considerar la introducción temprana de MTX, en particular para pacientes con alto riesgo de recaída y/o terapia prolongada, por ejemplo, pacientes mujeres con VSG inicial alta (>40 mm/h), artritis periférica y/o comorbilidades que pueden ser exacerbadas por la terapia con GC.
Los datos sobre el uso de azatioprina en el tratamiento de la PMR son muy limitados. A pesar de la evidencia limitada, la azatioprina se ha utilizado en algunos pacientes con PMR refractaria. Las recomendaciones ACR/EULAR para el tratamiento de la PMR no incluyen la azatioprina. Un estudio retrospectivo de baja calidad indicó que el agente antipalúdico hidroxicloroquina, que se usa para otras afecciones, no es eficaz para prevenir las recaídas en la PMR.
Dado que se ha demostrado que el anticuerpo monoclonal anti-receptor de IL-6 tocilizumab es eficaz para la ACG, existe una justificación para investigarlo como terapia para la PMR. Muchos informes de casos y series de casos sugieren la eficacia del tocilizumab intravenoso en pacientes individuales con PMR. Un estudio de cohorte retrospectivo del tratamiento con tocilizumab o MTX para la PMR recidivante en Japón indicó un efecto significativo de tocilizumab en la conservación de GC, pero no del MTX. Los ECA controlados con placebo de los inhibidores del TNF infliximab o etanercept no han demostrado ningún beneficio significativo en pacientes con PMR, por lo que no se recomiendan para el tratamiento de la PMR.
> Terapias de apoyo
El uso prolongado de GC es un factor importante que contribuye a varias comorbilidades en pacientes con enfermedades reumáticas, como vasculitis sistémica, PMR y ACG. Se recomienda que todos los pacientes con PMR reciban otras terapias de apoyo al inicio de su enfermedad, como calcio/vitamina D y bisfosfonatos para prevenir la osteoporosis.
Comorbilidades
Hay información limitada sobre comorbilidades en pacientes con PMR de grandes estudios epidemiológicos. En una revisión sistemática de la literatura, hubo algunas indicaciones de mayor riesgo de comorbilidades en pacientes con diagnóstico de PMR. Estas comorbilidades se pueden agrupar en enfermedad vascular, cáncer y otras enfermedades, incluyendo estas últimas el hipotiroidismo y enfermedad diverticular.
La comorbilidad más frecuente notificada tras el diagnóstico de PMR es la enfermedad vascular. Las condiciones vasculares incluyen apoplejía, infarto de miocardio y enfermedad vascular periférica. Esto está en consonancia con un mayor riesgo de enfermedad cardiovascular en otras enfermedades inflamatorias crónicas como la AR.
Si bien algunos estudios informaron un mayor riesgo de cáncer, otros informaron un riesgo menor o los resultados fueron equívocos. En cuanto a otras comorbilidades, hay datos contradictorios sobre una asociación con el hipotiroidismo. Hay algunos informes de un mayor riesgo de depresión, que puede estar asociado con el dolor crónico o el tratamiento de GC.
Los datos de un estudio de cohorte nacional reciente del Reino Unido respaldan el aumento del riesgo de enfermedad vascular después del diagnóstico de PMR. Además, también había riesgo de enfermedades respiratorias, renales y autoinmunes tras el diagnóstico de PMR. Al menos para los dos últimos, la explicación podría ser el sesgo de vigilancia.
Los pacientes con PMR tienen una alta tasa de comorbilidades asociadas con el tratamiento de GC, como osteoporosis, fracturas vertebrales, infecciones, cataratas y glaucoma. Sin embargo, en un estudio de cohorte en Olmstead, Minnesota, EE. UU., solo las cataratas fueron más comunes en pacientes con PMR seguidos durante una mediana de 5,8 años en comparación con los comparadores emparejados por edad y sexo sin PMR.
Posiblemente, el no aumento del riesgo de osteoporosis y fracturas podría reflejar el uso común de la profilaxis de la osteoporosis en este grupo de pacientes con tratamiento planificado a largo plazo con GC y con otros factores de riesgo de osteoporosis. Dichos patrones pueden depender del acceso a la atención en diferentes poblaciones.
Mortalidad
Dada la alta carga de comorbilidad entre los pacientes con PMR, es importante determinar si un diagnóstico de PMR se asocia con un mayor riesgo de mortalidad. Una revisión sistemática reciente encontró que los pacientes con PMR tenían una mayor carga de enfermedad comórbida en comparación con los controles emparejados por edad y sexo. Sin embargo, tres estudios previos informaron una reducción de la mortalidad entre los pacientes diagnosticados con PMR.
Una posible explicación para esto podría ser el sesgo de vigilancia. Los pacientes con enfermedades crónicas (y especialmente PMR donde se recomienda una evaluación, seguimiento y control regulares) tienen más probabilidades de estar bajo un seguimiento activo de su condición y cualquier morbilidad en desarrollo que conduzca al manejo de la enfermedad en una etapa temprana.
Otro estudio más, que se sabe que es el estudio más grande para estimar el efecto que tiene un diagnóstico de PMR en la esperanza de vida, mostró que un diagnóstico de PMR no tiene un impacto significativo en la esperanza de vida. Por lo tanto, un diagnóstico de PMR no parece aumentar el riesgo de muerte prematura.
Conclusión
- En conclusión, la PMR es un trastorno común y, a veces, un desafío clínico importante.
- Se necesitan más estudios sobre su fisiopatología para comprender mejor los mecanismos de la enfermedad como base para futuras terapias dirigidas.
- La inhibición de IL-6 es un concepto terapéutico particularmente prometedor, pero se necesitan más datos.
- Además, existe la necesidad de mejores métodos de diagnóstico, incluido un mayor desarrollo de modalidades de imagen, para facilitar el diagnóstico y el tratamiento adecuado.
Referencia bibliográfica
1 Raheel S, Shbeeb I, Crowson CS, Matteson EL. Epidemiology of polymyalgia rheumatica 2000–2014 and examination of incidence and survival trends over 45 years: a population-based study. Arthritis Care Res (Hoboken). 2017; 69: 1282– 5.
2 Doran MF, Crowson CS, O’Fallon WM, Hunder GG, Gabriel SE. Trends in the incidence of polymyalgia rheumatica over a 30 year period in Olmsted County, Minnesota, USA. J Rheumatol. 2002; 29: 1694– 7.
3 Michet CJ, Matteson EL. Polymyalgia rheumatica. BMJ. 2008; 336: 765– 9.
4 Gonzalez-Gay MA, Vazquez-Rodriguez TR, Lopez-Diaz MJ, Miranda-Filloy JA, Gonzalez-Juanatey C, Martin J, et al. Epidemiology of giant cell arteritis and polymyalgia rheumatica. Arthritis Rheum. 2009; 61: 1454– 61.
5 Noltorp S, Svensson B. High incidence of polymyalgia rheumatica and giant cell arteritis in a Swedish community. Clin Exp Rheumatol. 1991; 9: 351– 5.
6 Schaufelberger C, Bengtsson B-Å, Andersson R. Epidemiology and mortality in 220 patients with polymyalgia rheumatica. Br J Rheumatol. 1995; 34: 261– 4.
7 Gran JT, Myklebust G. The incidence of polymyalgia rheumatica and temporal arteritis in the county of Aust Agder, south Norway: a prospective study 1987–94. J Rheumatol. 1997; 24: 1739– 43.
8 Crowson CS, Matteson EL. Contemporary prevalence estimates for giant cell arteritis and polymyalgia rheumatica, 2015. Semin Arthritis Rheum. 2017; 47: 253– 6.
9 Salvarani C, Gabriel SE, O’Fallon WM, Hunder GG. The incidence of giant cell arteritis in Olmsted County, Minnesota: apparent fluctuations in a cyclic pattern. Ann Intern Med. 1995; 123: 192– 4.
10 Sharma A, Mohammad AJ, Turesson C. Incidence and prevalence of giant cell arteritis and polymyalgia rheumatica: a systematic literature review. Semin Arthritis Rheum. 2020; 50: 1040– 8.
11 Kim IY, Seo GH, Lee S, Jeong H, Kim H, Lee J, et al. Epidemiology of polymyalgia rheumatica in Korea. J Rheum Dis. 2014; 21: 297– 302.
12 Kobayashi S, Yano T, Matsumoto Y, Numano F, Nakajima N, Yasuda K, et al. Clinical and epidemiologic analysis of giant cell (temporal) arteritis from a nationwide survey in 1998 in Japan: the first government-supported nationwide survey. Arthritis Rheum. 2003; 49: 594– 8.
13 Cimmino MA, Zaccaria A. Epidemiology of polymyalgia rheumatica. Clin Exp Rheumatol. 2000; 18: S9– 11.
14 Cimmino MA. Genetic and environmental factors in polymyalgia rheumatica. Ann Rheum Dis. 1997; 56: 576– 7.
15 Metyas S, Chen C, Aung T, Ballester A, Cheav S. Rheumatologic manifestations of post SARS-CoV-2 infection: a case series. Curr Rheumatol Rev. 2022. https://doi.org/10.2174/1573397118666220211155716
16 Mettler C, Jonville-Bera A-P, Grandvuillemin A, Treluyer J-M, Terrier B, Chouchana L. Risk of giant cell arteritis and polymyalgia rheumatica following COVID-19 vaccination: a global pharmacovigilance study. Rheumatology (Oxford). 2022; 61: 865– 7.
17 Hysa E, Sobrero A, Camellino D, Rumi F, Carrara G, Cutolo M, et al. A seasonal pattern in the onset of polymyalgia rheumatica and giant cell arteritis? A systematic review and meta-analysis. Semin Arthritis Rheum. 2020; 50: 1131– 9.
18 Sobrero A, Paolino S, Hysa E, Camellino D, Tomatis V, Cutolo M, et al. Seasonal onset of polymyalgia rheumatica: correlations with the pattern of clinical presentation, disease severity and outcome in 383 patients from a single centre. Clin Exp Rheumatol. 2021; 39: 564– 9.
19 Peris P. Polymyalgia rheumatica is not seasonal in pattern and is unrelated to parvovirus b19 infection. J Rheumatol. 2003; 30: 2624– 6.
20 Liozon E, Parreau S, Filloux M, Dumonteil S, Gondran G, Bezanahary H, et al. Giant cell arteritis or polymyalgia rheumatica after influenza vaccination: a study of 12 patients and a literature review. Autoimmun Rev. 2021; 20:102732.
21 Izuka S, Komai T, Natsumoto B, Shoda H, Fujio K. Self-limited polymyalgia rheumatica-like syndrome following mRNA-1273 SARS-CoV-2 vaccination. Intern Med. 2022; 61: 903– 6.
22 Cadiou S, Perdriger A, Ardois S, Albert J-D, Berthoud O, Lescoat A, et al. SARS-CoV-2, polymyalgia rheumatica and giant cell arteritis: COVID-19 vaccine shot as a trigger? Comment on: “Can SARS-CoV-2 trigger relapse of polymyalgia rheumatica?” by Manzo Joint Bone Spine 2021;88:105150. Joint Bone Spine. 2022; 89:105282.
23 Meliconi R, Pulsatelli L, Uguccioni M, Salvarani C, Macchioni P, Melchiorri C, et al. Leukocyte infiltration in synovial tissue from the shoulder of patients with polymyalgia rheumatica. Quantitative analysis and influence of corticosteroid treatment. Arthritis Rheum. 1996; 39: 1199– 207.
24 Meliconi R, Pulsatelli L, Dolzani P, Boiardi L, Macchioni P, Salvarani C, et al. Vascular endothelial growth factor production in polymyalgia rheumatica. Arthritis Rheum. 2000; 43: 2472– 80.
25 Meliconi R, Pulsatelli L, Melchiorri C, Frizziero L, Salvarani C, Macchioni P, et al. Synovial expression of cell adhesion molecules in polymyalgia rheumatica. Clin Exp Immunol. 1997; 107: 494– 500.
26 Pulsatelli L, Dolzani P, Silvestri T, De Giorgio R, Salvarani C, Macchioni P, et al. Synovial expression of vasoactive intestinal peptide in polymyalgia rheumatica. Clin Exp Rheumatol. 2006; 24: 562– 6.
27 Ruta S, Rosa J, Navarta DA, Saucedo C, Catoggio LJ, Monaco RG, et al. Ultrasound assessment of new onset bilateral painful shoulder in patients with polymyalgia rheumatica and rheumatoid arthritis. Clin Rheumatol. 2012; 31: 1383– 7.
28 Owen CE, Poon AMT, Yang V, Mcmaster C, Lee ST, Liew DFL, et al. Abnormalities at three musculoskeletal sites on whole-body positron emission tomography/computed tomography can diagnose polymyalgia rheumatica with high sensitivity and specificity. Eur J Nucl Med Mol Imaging. 2020; 47: 2461– 8.
29 Shintani S, Shiigai T, Matsui Y. Polymyalgia rheumatica (PMR): clinical, laboratory, and immunofluorescence studies in 13 patients. Clin Neurol Neurosurg. 2002; 104: 20– 9.
30 Uddhammar A, Rantapaa Dahlqvist S, Hedberg B, Thornell LE. Deltoid muscle in patients with polymyalgia rheumatica. J Rheumatol. 1998; 25: 1344– 51.
31 Roche NE, Fulbright JW, Wagner AD, Hunder GG, Goronzy JJ, Weyand CM. Correlation of interleukin-6 production and disease activity in polymyalgia rheumatica and giant cell arteritis. Arthritis Rheum. 1993; 36: 1286– 94.
32 Samson M, Corbera-Bellalta M, Audia S, Planas-Rigol E, Martin L, Cid MC, et al. Recent advances in our understanding of giant cell arteritis pathogenesis. Autoimmun Rev. 2017; 16: 833– 44.
33 Pulsatelli L, Boiardi L, Pignotti E, Dolzani P, Silvestri T, Macchioni P, et al. Serum interleukin-6 receptor in polymyalgia rheumatica: a potential marker of relapse/recurrence risk. Arthritis Rheum. 2008; 59: 1147– 54.
34 Weyand CM, Goronzy JJ. Immune mechanisms in medium and large-vessel vasculitis. Nat Rev Rheumatol. 2013; 9: 731– 40.
35 Weyand CM, Hicok KC, Hunder GG, Goronzy JJ. Tissue cytokine patterns in patients with polymyalgia rheumatica and giant cell arteritis. Ann Intern Med. 1994; 121: 484– 91.
36 Carvajal Alegria G, Boukhlal S, Cornec D, Devauchelle-Pensec V. The pathophysiology of polymyalgia rheumatica, small pieces of a big puzzle. Autoimmun Rev. 2020; 19:102670.
37 Van Sleen Y, Wang Q, Van Der Geest KSM, Westra J, Abdulahad WH, Heeringa P, et al. Involvement of monocyte subsets in the immunopathology of giant cell arteritis. Sci Rep. 2017; 7: 6553.
38 Hysa E, Gotelli E, Sammorì S, Cimmino MA, Paolino S, Pizzorni C, et al. Immune system activation in polymyalgia rheumatica: which balance between autoinflammation and autoimmunity? A systematic review. Autoimmun Rev. 2022; 21:102995.
39 Jakobsson K, Jacobsson L, Warrington K, Matteson EL, Liang K, Melander O, et al. Body mass index and the risk of giant cell arteritis: results from a prospective study. Rheumatology (Oxford). 2015; 54: 433– 40.
40 Wadström K, Jacobsson L, Mohammad AJ, Warrington KJ, Matteson EL, Turesson C. Negative associations for fasting blood glucose, cholesterol and triglyceride levels with the development of giant cell arteritis. Rheumatology (Oxford). 2020; 59: 3229– 36.
41 Salvarani C, Cantini F, Hunder GG. Polymyalgia rheumatica and giant-cell arteritis. Lancet. 2008; 372: 234– 45.
42 Salvarani C, Cantini F, Boiardi L, Hunder GG. Polymyalgia rheumatica. Best Pract Res Clin Rheumatol. 2004; 18: 705– 22.
43 Nesher G. Polymyalgia rheumatica—diagnosis and classification. J Autoimmun. 2014; 48–49: 76– 8.
44 Kermani TA, Warrington KJ. Polymyalgia rheumatica. Lancet. 2013; 381: 63– 72.
45 Twohig H, Mitchell C, Mallen C, Adebajo A, Mathers N. “I suddenly felt I’d aged”: a qualitative study of patient experiences of polymyalgia rheumatica (PMR). Patient Educ Couns. 2015; 98: 645– 50.
46 Salvarani C, Gabriel SE, Michael O’fallon W, Hunder GG. Epidemiology of polymyalgia rheumatica in Olmsted County, Minnesota, 1970–1991. Arthritis Rheum. 1995; 38: 369– 73.
47 Hamrin B, Jonsson N, Hellsten S. “Polymyalgia arteritica”. Further clinical and histopathological studies with a report of six autopsy cases. Ann Rheum Dis. 1968; 27: 397– 405.
48 Schmidt WA, Gromnica-Ihle E. Incidence of temporal arteritis in patients with polymyalgia rheumatica: a prospective study using colour Doppler ultrasonography of the temporal arteries. Rheumatology (Oxford). 2002; 41: 46– 52.
49 Baldursson Ó, Steinsson K, Björnsson J, Lie JT. Giant cell arteritis in Iceland. An epidemiologic and histopathologic analysis. Arthritis and Rheumatism. 1994; 37: 1007– 12.
50 Gonzalez-Gay MA, García-Porrúa C. Systemic vasculitis in adults in northwestern Spain, 1988–1997. Clinical and epidemiologic aspects. Medicine (Baltimore). 1999; 78: 292– 308.
51 Kermani TA, Warrington KJ, Cuthbertson D, Carette S, Hoffman GS, Khalidi NA, et al. Disease relapses among patients with giant cell arteritis: a prospective, longitudinal cohort study. J Rheumatol. 2015; 42: 1213– 7.
52 Nobunaga M, Yoshioka K, Yasuda M, Shingu M. Clinical studies of polymyalgia rheumatica. A proposal of diagnostic criteria. Jpn J Med. 1989; 28: 452– 6.
53 Bird HA, Esselinckx W, Dixon AS, Mowat AG, Wood PH. An evaluation of criteria for polymyalgia rheumatica. Ann Rheum Dis. 1979; 38: 434– 9.
54 Healey LA. Long-term follow-up of polymyalgia rheumatica: evidence for synovitis. Semin Arthritis Rheum. 1984; 13: 322– 8.
55 Hamrin B. Polymyalgia arteritica. Acta Med Scand Suppl. 1972; 533: 1– 131.
56 Chuang TY, Hunder GG, Ilstrup DM, Kurland LT. Polymyalgia rheumatica: a 10-year epidemiologic and clinical study. Ann Intern Med. 1982; 97: 672– 80.
57 Fors C, Bergström U, Willim M, Pilman E, Turesson C. Validity of polymyalgia rheumatica diagnoses and classification criteria in primary health care. Rheumatol Adv Pract. 2019; 3:rkz033.
58 Dasgupta B, Cimmino MA, Maradit-Kremers H, Schmidt WA, Schirmer M, Salvarani C, et al. 2012 provisional classification criteria for polymyalgia rheumatica: a European League Against Rheumatism/American College of Rheumatology collaborative initiative. Ann Rheum Dis. 2012; 71: 484– 92.
59 Figus FA, Skoczynska M, McConnell R, Massazza G, Iagnocco A. Imaging in polymyalgia rheumatica: which technique to use? Clin Exp Rheumatol. 2021; 39: 883– 8.
60 Mackie SL, Koduri G, Hill CL, Wakefield RJ, Hutchings A, Loy C, et al. Accuracy of musculoskeletal imaging for the diagnosis of polymyalgia rheumatica: systematic review. RMD Open. 2015; 1:e000100.
61 Frediani B, Falsetti P, Storri L, Bisogno S, Baldi F, Campanella V, et al. Evidence for synovitis in active polymyalgia rheumatica: sonographic study in a large series of patients. J Rheumatol. 2002; 29: 123– 30.
62 Lange U, Piegsa M, Teichmann J, Neeck G. Ultrasonography of the glenohumeral joints—a helpful instrument in differentiation in elderly onset rheumatoid arthritis and polymyalgia rheumatica. Rheumatol Int. 2000; 19: 185– 9.
63 Falsetti P, Acciai C, Volpe A, Lenzi L. Ultrasonography in early assessment of elderly patients with polymyalgic symptoms: a role in predicting diagnostic outcome? Scand J Rheumatol. 2011; 40: 57– 63.
64 Mackie SL, Pease CT, Fukuba E, Harris E, Emery P, Hodgson R, et al. Whole-body MRI of patients with polymyalgia rheumatica identifies a distinct subset with complete patient-reported response to glucocorticoids. Ann Rheum Dis. 2015; 74: 2188– 92.
65 Laporte J-P, Garrigues F, Huwart A, Jousse-Joulin S, Marhadour T, Guellec D, et al. Localized myofascial inflammation revealed by magnetic resonance imaging in recent-onset polymyalgia rheumatica and effect of tocilizumab therapy. J Rheumatol. 2019; 46: 1619– 26.
66 Van Der Geest KSM, Treglia G, Glaudemans AWJM, Brouwer E, Jamar F, Slart RHJA, et al. Diagnostic value of [18F]FDG-PET/CT in polymyalgia rheumatica: a systematic review and meta-analysis. Eur J Nucl Med Mol Imaging. 2021; 48: 1876– 89.
67 Yuge S, Nakatani K, Yoshino K, Koyama T. Diagnosing polymyalgia rheumatica on (18)F-FDG PET/CT: typical uptake patterns. Ann Nucl Med. 2018; 32: 573– 7.
68 Sondag M, Guillot X, Verhoeven F, Blagosklonov O, Prati C, Boulahdour H, et al. Utility of 18F-fluoro-dexoxyglucose positron emission tomography for the diagnosis of polymyalgia rheumatica: a controlled study. Rheumatology (Oxford). 2016; 55: 1452– 7
69 Richter MD, Crowson C, Kottschade LA, Finnes HD, Markovic SN, Thanarajasingam U. Rheumatic syndromes associated with immune checkpoint inhibitors: a single-center cohort of sixty-one patients. Arthritis Rheumatol. 2019; 71: 468– 75.
70 Calabrese C, Cappelli LC, Kostine M, Kirchner E, Braaten T, Calabrese L. Polymyalgia rheumatica-like syndrome from checkpoint inhibitor therapy: case series and systematic review of the literature. RMD Open. 2019; 5:e000906.
71 Zhang H, Watanabe R, Berry GJ, Vaglio A, Liao YJ, Warrington KJ, et al. Immunoinhibitory checkpoint deficiency in medium and large vessel vasculitis. Proc Natl Acad Sci U S A. 2017; 114: E970– 9.
72 Dejaco C, Singh YP, Perel P, Hutchings A, Camellino D, Mackie S, et al. 2015 Recommendations for the management of polymyalgia rheumatica: a European League Against Rheumatism/American College of Rheumatology collaborative initiative. Ann Rheum Dis. 2015; 74: 1799– 807.
73 Dejaco C, Singh YP, Perel P, Hutchings A, Camellino D, Mackie S, et al. Current evidence for therapeutic interventions and prognostic factors in polymyalgia rheumatica: a systematic literature review informing the 2015 European League Against Rheumatism/American College of Rheumatology recommendations for the management of polymyalgia rheumatica. Ann Rheum Dis. 2015; 74: 1808– 17.
74 Kyle V, Hazleman BL. Treatment of polymyalgia rheumatica and giant cell arteritis. I. Steroid regimens in the first two months. Ann Rheum Dis. 1989; 48: 658– 61.
75 Floris A, Piga M, Chessa E, Congia M, Erre GL, Angioni MM, et al. Long-term glucocorticoid treatment and high relapse rate remain unresolved issues in the real-life management of polymyalgia rheumatica: a systematic literature review and meta-analysis. Clin Rheumatol. 2021; 41(1): 19– 31.
76 Dasgupta B, Gray J, Fernandes L, Olliff C. Treatment of polymyalgia rheumatica with intramuscular injections of depot methylprednisolone. Ann Rheum Dis. 1991; 50: 942– 5.
77 Dasgupta B, Dolan AL, Panayi GS, Fernandes L. An initially double-blind controlled 96 week trial of depot methylprednisolone against oral prednisolone in the treatment of polymyalgia rheumatica. Br J Rheumatol. 1998; 37: 189– 95.
78 Caporali R, Cimmino MA, Ferraccioli G, Gerli R, Klersy C, Salvarani C, et al. Prednisone plus methotrexate for polymyalgia rheumatica: a randomized, double-blind, placebo-controlled trial. Ann Intern Med. 2004; 141: 493– 500.
79 Ferraccioli G, Salaffi F, De Vita S, Casatta L, Bartoli E. Methotrexate in polymyalgia rheumatica: preliminary results of an open, randomized study. J Rheumatol. 1996; 23: 624– 8.
80 Dejaco C, Singh YP, Perel P, Hutchings A, Camellino D, Mackie S, et al. 2015 Recommendations for the management of polymyalgia rheumatica: a European League Against Rheumatism/American College of Rheumatology collaborative initiative. Ann Rheum Dis. 2015; 74: 1799– 807.
81 De Silva M, Hazleman BL. Azathioprine in giant cell arteritis/polymyalgia rheumatica: a double-blind study. Ann Rheum Dis. 1986; 45: 136– 8.
82 Lee JH, Choi ST, Kim JS, Yoon BY, Kwok S-K, Kim H-S, et al. Clinical characteristics and prognostic factors for relapse in patients with polymyalgia rheumatica (PMR). Rheumatol Int. 2013; 33: 1475– 80.
83 Stone JH, Klearman M, Collinson N. Trial of tocilizumab in giant-cell arteritis. N Engl J Med. 2017; 377: 1494– 5.
84 Akiyama M, Kaneko Y, Takeuchi T. Tocilizumab in isolated polymyalgia rheumatica: a systematic literature review. Semin Arthritis Rheum. 2020; 50: 521– 5.
85 Spiera R, Unizony SH, Bao M, Luder Y, Han J, Pavlov A, et al. Tocilizumab vs placebo for the treatment of giant cell arteritis with polymyalgia rheumatica symptoms, cranial symptoms or both in a randomized trial. Semin Arthritis Rheum. 2021; 51: 469– 76.
86 Izumi K, Murata O, Higashida-Konishi M, Kaneko Y, Oshima H, Takeuchi T. Steroid-sparing effect of tocilizumab and methotrexate in patients with polymyalgia rheumatica: a retrospective cohort study. J Clin Med. 2021; 10: 2948.
87 Salvarani C, Macchioni P, Manzini C, Paolazzi G, Trotta A, Manganelli P, et al. Infliximab plus prednisone or placebo plus prednisone for the initial treatment of polymyalgia rheumatica: a randomized trial. Ann Intern Med. 2007; 146: 631– 9.
88 Kreiner F, Galbo H. Effect of etanercept in polymyalgia rheumatica: a randomized controlled trial. Arthritis Res Ther. 2010; 12: R176.
89 Mazzantini M, Torre C, Miccoli M, Baggiani A, Talarico R, Bombardieri S, et al. Adverse events during longterm low-dose glucocorticoid treatment of polymyalgia rheumatica: a retrospective study. J Rheumatol. 2012; 39: 552– 7.
90 Proven A, Gabriel SE, Orces C, O’Fallon WM, Hunder GG. Glucocorticoid therapy in giant cell arteritis: duration and adverse outcomes. Arthritis Rheum. 2003; 49: 703– 8.
91 Robson J, Doll H, Suppiah R, Flossmann O, Harper L, Höglund P, et al. Damage in the anca-associated vasculitides: long-term data from the European vasculitis study group (EUVAS) therapeutic trials. Ann Rheum Dis. 2015; 74: 177– 84.
92 Gabriel SE, Sunku J, Salvarani C, O’Fallon WM, Hunder GG. Adverse outcomes of antiinflammatory therapy among patients with polymyalgia rheumatica. Arthritis Rheum. 1997; 40: 1873– 8.
93 Strehl C, Bijlsma JWJ, De Wit M, Boers M, Caeyers N, Cutolo M, et al. Defining conditions where long-term glucocorticoid treatment has an acceptably low level of harm to facilitate implementation of existing recommendations: viewpoints from an EULAR task force. Ann Rheum Dis. 2016; 75: 952– 7.
94 Buckley L, Guyatt G, Fink HA, Cannon M, Grossman J, Hansen KE, et al. 2017 American College of Rheumatology guideline for the prevention and treatment of glucocorticoid-induced osteoporosis. Arthritis Care Res (Hoboken). 2017; 69: 1095– 110.
95 Partington R, Helliwell T, Muller S, Abdul Sultan A, Mallen C. Comorbidities in polymyalgia rheumatica: a systematic review. Arthritis Res Ther. 2018; 20: 258.
96 Partington R, Muller S, Mallen CD, Abdul Sultan A, Helliwell T. Comorbidities in patients with polymyalgia rheumatica prior to and following diagnosis: a case control and cohort study. Semin Arthritis Rheum. 2020; 50: 663– 72.
97 Shbeeb I, Challah D, Raheel S, Crowson CS, Matteson EL. Comparable rates of glucocorticoid-associated adverse events in patients with polymyalgia rheumatica and comorbidities in the general population. Arthritis Care Res (Hoboken). 2018; 70: 643– 7.
98 Gran JT, Myklebust G, Wilsgaard T, Jacobsen BK. Survival in polymyalgia rheumatica and temporal arteritis: a study of 398 cases and matched population controls. Rheumatology (Oxford). 2001; 40: 1238– 42.
99 Myklebust G, Wilsgaard T, Koster Jacobsen B, Tore Gran J. Causes of death in polymyalgia rheumatica. A prospective longitudinal study of 315 cases and matched population controls. Scand J Rheumatol. 2003; 32: 38– 41.
100 Uddhammar A, Eriksson AL, Nystrom L, Stenling R, Rantapää-Dahlqvist S. Increased mortality due to cardiovascular disease in patients with giant cell arteritis in northern Sweden. J Rheumatol. 2002; 29: 737– 42.
101 Partington R, Muller S, Mallen CD, Abdul Sultan A, Helliwell T. Mortality among patients with polymyalgia rheumatica: a retrospective cohort study. Arthritis Care Res (Hoboken). 2021; 73: 1853– 7.
102 Kyle V, Hazleman BL. Treatment of polymyalgia rheumatica and giant cell arteritis. II. Relation between steroid dose and steroid associated side effects. Ann Rheum Dis. 1989; 48: 662– 6.
103 Caporali R, Cimmino MA, Ferraccioli G, Gerli R, Klersy C, Salvarani C, et al. Prednisone plus methotrexate for polymyalgia rheumatica: a randomized, double-blind, placebo-controlled trial. Ann Intern Med. 2004; 141: 493– 500.
Fuente: https://www.intramed.net/contenidover.asp?contenidoid=101727

